L’introduction de ChatGPT a attiré l’attention du monde sur la puissance de l’intelligence artificielle générative et ses applications dans tous les secteurs. Bien que le potentiel de l’IA appliquée aux workflows de découverte de médicaments soit connu depuis des années, l’accent et l’enthousiasme suscités par les grands modèles génératifs accéléreront considérablement l’adoption et la validation de ces outils pour la découverte biologique.
Les premiers résultats démontrent que la transition vers les modèles génératifs est un point d’inflexion pour l’industrie. Les applications de grands modèles de langage (LLM) pour l’identification cible et générative des pistes accélèrent notre compréhension de la biologie et améliorent la qualité des candidats-médicaments initiaux. Des représentations de meilleure qualité des médicaments et de leurs cibles améliorent aujourd’hui notre capacité à prédire les propriétés des médicaments et leurs interactions.
Dépasser un statu quo inférieur aux normes dans la découverte de médicaments
L’amélioration de la vitesse et de la qualité des pipelines de découverte de médicaments précliniques précoces est directement liée au déblocage de nouvelles thérapies pour améliorer les résultats des patients et sauver des vies. La découverte de médicaments traditionnels prend du temps et coûte cher. Une fois qu’une cible médicamenteuse a été identifiée et optimisée, la probabilité d’une mise sur le marché réussie est inférieure à 10 %.
Même de petites avancées dans l’optimisation du délai d’exécution et les améliorations de la probabilité de succès clinique sont importantes pour traiter les milliers de maladies qui n’ont aujourd’hui aucun traitement ou remède connu.
Les grands modèles de langage apprennent le langage de la biologie
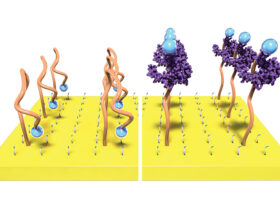
Les modèles d’IA générative d’aujourd’hui comprennent le langage de la biologie, de la chimie et de la génomique, tirant parti de nombreux outils qui ont été développés au cours des dernières années et qui ont conduit à l’avènement de ChatGPT et d’autres LLM. Bien que ces modèles aient déjà été appliqués aux données de séquence biopharmaceutiques (par exemple, la modélisation à l’échelle évolutive formée sur de grandes bases de données de séquences de protéines), le succès démontré d’AlphaFold de Google DeepMind a été le moment décisif démontrant la promesse de ces outils.
Depuis lors, la croissance exponentielle de la recherche et du développement dans l’espace est difficile à ignorer : pratiquement chaque semaine, de nouvelles architectures, modèles et approches de pointe sont publiés et mis à disposition, du milieu universitaire à l’industrie. Par exemple, DiffDock a été récemment publié, qui a démontré le premier outil viable d’amarrage de protéines à petites molécules basé sur l’IA. Le cas échéant, ce modèle accélère les commandes pour les flux de travail d’amarrage, conduisant à des flux de travail de criblage de petites molécules moins chers et plus efficaces.
L’IA générative est une prescription pour le succès des soins de santé
Chaque étape du pipeline de découverte de médicaments par IA est accélérée grâce à l’IA. Les LLM parcourent la littérature pour découvrir de nouvelles cibles médicamenteuses. Les modèles génératifs entraînés sur des données de petites molécules et de protéines fournissent des outils pour générer virtuellement des candidats-médicaments aux propriétés définies (et, dans un récent article conjoint entre NVIDIA et Evozyne, ont été synthétisés et validés en laboratoire).
Les flux de travail d’apprentissage de représentation, tels que ceux pris en charge par les modèles à l’échelle évolutive dans la conception de protéines, fournissent les outils de prédiction de propriétés de la plus haute qualité encore connus dans le domaine et contribuent directement à la performance des outils de prédiction de structure tels qu’AlphaFold et ESMFold. Les applications de ces modèles à la génomique ont conduit au premier véritable modèle de base généralisable pour des tâches telles que la prédiction de l’expression des gènes, récemment publié par NVIDIA, l’Université technique de Munich et InstaDeep (acquis cette année par BioNTech).
Nous sommes à un point d’inflexion majeur pour l’utilisation de l’IA dans la découverte précoce de médicaments, mais il en va de même pour les essais cliniques. Si nous disposons de formidables outils génératifs et prédictifs pour les médicaments et leurs cibles, comment structurer plus efficacement un essai clinique pour maximiser ses chances de succès pour un candidat-médicament donné ?
Des outils qui intègrent les données multimodales des patients, les dossiers de santé électroniques, la génomique et d’autres représentations de la santé humaine et de la biologie sont en cours de construction aujourd’hui pour recruter plus efficacement et plus efficacement des patients dans des essais cliniques et pour les aider à trouver eux-mêmes des essais.
Les capacités de l’IA générative à comprendre des relations complexes en langage naturel sont désormais, pour la première fois, généralement comprises par des centaines de millions de personnes dans le monde. L’impact de l’IA générative sur la biologie et la découverte de médicaments améliorera bientôt la vie des gens partout dans le monde.